Lupus Eritematosus Sistemik Adalah Penyakit Autoimun Sistemik – Lupus eritematosus sistemik (LES) adalah penyakit autoimun sistemik dengan keterlibatan multisistem dan dikaitkan dengan morbiditas dan mortalitas yang signifikan. Faktor genetik, imunologi, endokrin, dan lingkungan mempengaruhi hilangnya toleransi imunologis terhadap antigen diri yang mengarah pada pembentukan autoantibodi patogen yang menyebabkan kerusakan jaringan melalui berbagai mekanisme. Kegiatan ini meninjau evaluasi dan manajemen lupus eritematosus sistemik dan menyoroti peran tim interprofessional dalam merawat pasien dengan kondisi ini.
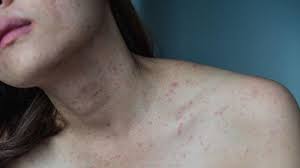
Lupus Eritematosus Sistemik Adalah Penyakit Autoimun Sistemik
Tujuan:
Jelaskan kapan harus mempertimbangkan lupus eritematosus sistemik pada diagnosis banding.
Jelaskan evaluasi lupus eritematosus sistemik.
Jelaskan pilihan pengobatan untuk lupus eritematosus sistemik.
Jelaskan pentingnya pendekatan interprofessional untuk meningkatkan kesadaran, diagnosis yang akurat, dan pengobatan yang cepat untuk meningkatkan perawatan pasien dengan lupus eritematosus sistemik.
pengantar
Lupusmn.org – Lupus eritematosus sistemik (LES) adalah penyakit autoimun sistemik, dengan keterlibatan multisistemik. Penyakit ini memiliki beberapa fenotipe, dengan berbagai presentasi klinis pada pasien mulai dari manifestasi mukokutan ringan hingga multiorgan dan keterlibatan sistem saraf pusat yang parah. Beberapa jalur imunopatogenik berperan dalam perkembangan SLE. Lupus eritematosus (sel LE) dijelaskan oleh Hargraves pada tahun 1948. Beberapa autoantibodi patogen telah diidentifikasi. Meskipun kemajuan terbaru dalam teknologi dan pemahaman tentang dasar patologis dan faktor risiko SLE, patogenesis pasti SLE masih belum diketahui dengan baik. Diagnosis SLE dapat menjadi tantangan dan sementara beberapa kriteria klasifikasi telah diajukan, kegunaannya dalam pengaturan klinis masih menjadi bahan perdebatan.
Baca Juga : Hidup Berdampingan Dengan Lupus
Etiologi
SLE merupakan penyakit multifaktorial dengan etiologi yang belum diketahui pasti, namun beberapa faktor genetik, imunologi, endokrin, dan lingkungan berperan dalam etiopatogenesis SLE.
Segregasi familial dan tingkat konkordansi yang tinggi pada kembar identik menunjukkan kontribusi genetik yang kuat pada SLE, meskipun tidak ada pola pewarisan yang jelas. Tingkat yang sesuai untuk kembar identik telah dilaporkan setinggi 50%. Lebih dari 50 gen atau lokus genomik telah diidentifikasi terkait dengan SLE, sebagian besar protein penyandi terlibat dalam fungsi sistem kekebalan. [2] Gen-gen ini berhubungan dengan aktivasi sistem imun sebagai respons terhadap antigen asing, pembentukan antigen sendiri, dan aktivasi sistem imun bawaan dan adaptif. Beberapa mutasi gen yang jarang terjadi, tetapi dianggap berisiko sangat tinggi untuk perkembangan SLE termasuk defisiensi komponen pelengkap awal C1q, C1r, C1s (risiko>90%), C4 (50%), C2 (20%) dan TREX1. Beberapa gen lain yang terkait termasuk HLA-DRB1, HLA-DR2, HLA-DR3, HLA-DRX, TNFAIP3, STAT-4, STAT-1, TLR-7, IRAK1/MECP2, IRF5-TNPO3, ITGAM, dll. Wanita berisiko 10 kali lebih besar terkena SLE daripada pria, dan risiko SLE 14 kali lebih besar pada sindrom Klinefelter (47, XXY). Ini menunjukkan hubungan dengan gen pada kromosom X, namun, meskipun beberapa penelitian, gen yang tepat belum diidentifikasi.
Jenis kelamin wanita dan pengaruh hormonal merupakan faktor risiko yang signifikan untuk SLE. Estrogen dan prolaktin meningkatkan autoimunitas dan meningkatkan produksi faktor aktivasi sel B dan memodulasi aktivasi limfosit dan pDC. Penggunaan kontrasepsi yang mengandung estrogen dan terapi penggantian hormon pascamenopause dapat menyebabkan flare pada pasien SLE dan telah dikaitkan dengan insiden SLE yang lebih tinggi. Peningkatan kadar prolaktin terlihat pada pasien dengan SLE. Androgen, di sisi lain, dianggap protektif.
Beberapa pemicu lingkungan dari SLE telah diidentifikasi. Beberapa obat telah terlibat dalam menyebabkan fenomena mirip lupus dengan menyebabkan demetilasi DNA dan perubahan antigen diri. [3] Sementara procainamide dan hydralazine memiliki insiden tertinggi menyebabkan lupus yang diinduksi obat, lebih dari 100 obat telah dikaitkan dengan lupus yang diinduksi obat. Lebih lanjut, beberapa obat seperti obat sulfa diketahui menyebabkan flare pada pasien SLE. Sinar ultraviolet dan paparan sinar matahari menyebabkan peningkatan apoptosis sel dan merupakan salah satu pemicu SLE yang terkenal. Beberapa infeksi virus telah terlibat, mekanisme yang mendasari dianggap mimikri molekuler. Antibodi terhadap virus Epstein-Barr (EBV) lebih umum pada anak-anak dan orang dewasa dengan SLE dibandingkan dengan populasi umum. Merokok juga dianggap sebagai risiko, dengan respons dosis. [4] Faktor risiko potensial lainnya termasuk paparan silika, infeksi virus lainnya, kekurangan vitamin D, kecambah alfalfa dan makanan yang mengandung canavanine.
Epidemiologi
Berbagai prevalensi dan tingkat kejadian SLE telah dilaporkan, dengan perbedaan sebagian besar disebabkan oleh perbedaan populasi. Registri lupus Georgia dan Michigan melaporkan prevalensi 72,1 hingga 74,4 per 100.000 orang dan tingkat kejadian 5,6 per 100.000 orang-tahun terutama pada populasi Kaukasia dan Afrika-Amerika. Afrika-Amerika memiliki tingkat tertinggi, dan tingkat lebih tinggi di antara populasi Asia dan Hispanik dibandingkan dengan Kaukasia. Penyakit ini cenderung memiliki onset usia yang lebih dini dan lebih parah pada orang Afrika-Amerika.
SLE terutama menyerang wanita usia subur, dengan rasio wanita dan pria 9 banding 1. Namun, risikonya menurun setelah menopause pada wanita meskipun masih dua kali lipat dibandingkan pria. Penelitian telah menunjukkan bahwa meskipun jarang, lupus pada pria cenderung lebih parah.
Usia memainkan peran penting dalam SLE, dan meskipun penyakit ini lebih sering terjadi pada usia subur pada wanita, telah dilaporkan dengan baik pada populasi anak dan lansia. SLE lebih parah pada anak-anak sedangkan pada orang tua, cenderung lebih berbahaya dan memiliki lebih banyak keterlibatan paru dan serositis dan lebih sedikit Raynaud, ruam malar, nefritis, dan komplikasi neuropsikiatri.
Patofisiologi
Patogenesis SLE sangat kompleks, dan pemahaman tentang patogenesis SLE terus berkembang. Sebuah istirahat dalam toleransi pada individu yang rentan secara genetik, pada paparan faktor lingkungan, menyebabkan aktivasi autoimunitas. Kerusakan sel yang disebabkan oleh infeksi dan faktor lingkungan lainnya memaparkan sistem kekebalan terhadap antigen diri yang mengarah pada aktivasi sel T dan B yang menjadi mandiri oleh respons imun yang bertujuan sendiri secara kronis. Pelepasan sitokin, aktivasi komplemen, dan produksi autoantibodi kemudian menyebabkan kerusakan organ.
Baik sistem imun bawaan maupun adaptif berperan dalam patogenesis SLE. Aktivasi sistem imun bawaan bergantung pada Toll-like receptor (TLR), atau independen. TLR terikat membran sel (TLR 2, 4, 6) diaktifkan pada paparan DNA ekstraseluler dan RNA dari sel yang sekarat, yang mengarah ke aktivasi hilir dari keluarga pengatur Interferon (IRF-3), NF-κB dan MAP- kinase, yang berfungsi sebagai faktor transkripsi untuk produksi mediator proinflamasi seperti IFN-b. TLR endosomal (TLR 7, 9) diaktifkan oleh RNA untai tunggal dan DNA demetilasi dan mengarah pada produksi interferon-alfa, dan autoantibodi pengikat RNA seperti antibodi terhadap Ro, La, Sm, dan RNP. Jalur TLR-independen diaktifkan oleh sensor RNA intracytoplasmic (RIG-1, MDA-5) dan sensor DNA (IFI16, DAI) dan menyebabkan aktivasi IRF3 dan NF-κB. Baik DNA/RNA diri maupun DNA/RNA asing seperti dari virus dapat menyebabkan aktivasi ini. NETosis baru-baru ini mendapat perhatian dalam patogenesis SLE. Neutrofil, pada aktivasi oleh berbagai faktor seperti sitokin, trombosit teraktivasi dan sel endotel vaskular secara sistematis melepaskan agregat nuklir mereka di lingkungan ekstraseluler. Agregat nuklir ini kemudian dapat meningkatkan produksi Interferon-alfa oleh sel dendritik, memediasi trombosis dan kerusakan pembuluh darah dan berfungsi sebagai antigen sendiri untuk limfosit T. trombosit teraktivasi dan sel endotel vaskular secara sistematis melepaskan agregat inti mereka di lingkungan ekstraseluler. Agregat nuklir ini kemudian dapat meningkatkan produksi Interferon-alfa oleh sel dendritik, memediasi trombosis dan kerusakan pembuluh darah dan berfungsi sebagai antigen sendiri untuk limfosit T. trombosit teraktivasi dan sel endotel vaskular secara sistematis melepaskan agregat inti mereka di lingkungan ekstraseluler. Agregat nuklir ini kemudian dapat meningkatkan produksi Interferon-alfa oleh sel dendritik, memediasi trombosis dan kerusakan pembuluh darah dan berfungsi sebagai antigen sendiri untuk limfosit T.
Limfosit T dan limfosit B memainkan peran penting dalam patogenesis SLE. Antigen yang diturunkan dari sel yang mengalami apoptosis dan rusak dipresentasikan ke sel T oleh sel penyaji antigen. Sel-T dalam SLE menampilkan ekspresi gen yang terdistorsi yang mengarah ke produksi beberapa sitokin. Sel T ini menghasilkan lebih sedikit IL-2, yang mengarah pada perubahan produksi sel T regulator. Peningkatan IL-6, IL-10, IL-12 dan IL-23 meningkatkan produksi sel mononuklear sementara peningkatan IL-17 dan IL-21 menyebabkan peningkatan produksi sel T. Peningkatan Interfern-γ menyebabkan produksi sel T yang rusak. Sel T menyebabkan aktivasi sel B autoreaktif oleh CD40L dan produksi sitokin, yang mengarah pada produksi autoantibodi, yang merupakan ciri khas SLE. Reseptor seperti tol pada interaksi dengan DNA dan RNA menyebabkan aktivasi sel-B ini, dan kompleks intranuklear yang mengandung asam nukleat dan protein adalah antigen paling menonjol yang menyebabkan aktivasi sel-B. Autoantibodi ini bersifat patogen dan menyebabkan kerusakan organ melalui deposisi kompleks imun, komplemen, dan aktivasi neutrofil, serta mengubah fungsi sel yang mengarah pada apoptosis dan produksi sitokin. Lebih lanjut, sel B autoreaktif dalam SLE yang dirangsang oleh antigen sendiri, tidak segera dihilangkan karena kekurangan proses yang terlibat dalam netralisasi fungsional sel B autoreaktif. Sel B juga dapat berfungsi sebagai sel penyaji antigen dan dapat mengaktifkan sel T dengan menghadirkan antigen terlarut yang diinternalisasi ke sel T. Ini menciptakan lingkaran di mana sel B dan T saling mengaktifkan, keduanya mengarah ke lebih banyak autoimunitas.
